Новости
Делегация Росстандарта во главе с руководителем ведомства Антоном Шалаевым посетила опорную лабораторию, которая позволит проводить испытания продукции, поставляемой на экспорт, открывшуюся в Государственном центре стандартизации, метрологии и испытаний (ЦСМ) в Ростовской области.
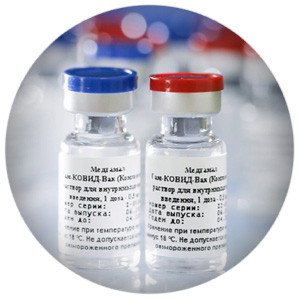
Экспорт вакцин из России по итогам 2021 года составил 1,42 млрд долл. и продолжает увеличиваться, следует из статистики Федеральной таможенной службы. В 2020 году было вывезено этих препаратов на 72 млн долл.
В 1988 году журналисты выяснили, что компания Минкова фактически не существует, а для выхода на IPO тот подделал несколько десятков тысяч документов. Обозреватель vc.ru рассказал историю Барри Минкова, который, выйдя из тюрьмы, снова попал туда за обман нескольких членов своего церковного прихода.
Мировой рынок лекарств, которые напечатаны на 3D-принтере, оценивается в 201,74 миллиона долларов США в 2021 году. Ожидается, что он достигнет 336,89 миллиона долларов США к 2026 году. Увеличение в среднем составит 10,8% в год.
Росстат опубликовал статистику «О промышленном производстве» в 2021 году из которой следует, что производство лекарственных средств и материалов, применяемых в медицинских целях, в России по итогам 2021 года увеличилось на 11,5% по сравнению с 2020 годом.
15 февраля состоится закрытое онлайн заседание РАФМ по теме: «Фармацевтический рынок России. Итоги 2021 года».
XVII Международная конференция «Фармацевтический бизнес в России — 2022» состоится 10 марта 2022 г. в Москве, отель Radisson Collection.
В развитие площадки планируется вложить 815 млн рублей, 500 из которых – безвозвратные деньги федерального бюджета
Постановление от 29.12.2021 № 2544 о внесении изменений в государственную программу Российской Федерации «Развитие фармацевтической и медицинской промышленности» опубликовано на Официальном интернет-портале правовой информации.
В 2022 году в особой экономической зоне (ОЭЗ) «Технополис «Москва» будет запущено не менее десяти производств, в том числе лекарств.
По данным Росстат выпуск лекарственных средств и материалов, применяемых в медицинских целях, в ноябре 2021 года увеличился на 8,6% по сравнению с аналогичным периодом 2020 года. По сравнению с октябрем 2021 года производство увеличилось на 4,2% . За одиннадцать месяцев 2021 года производство этих видов продукции увеличилось на 18,6% по сравнению с январем–ноябрем прошлого года.
Коллегия Евразийской экономической комиссии обновила позиции классификатора видов документов регистрационного досье лекарственного препарата и справочника структурных элементов регистрационного досье лекарственного препарата с учетом актуальной редакции Правил регистрации и экспертизы лекарственных средств для медицинского применения, утвержденных Решением Совета Комиссии от 3 ноября 2016 г. № 78.
Министр экономического развития и инвестиционной политики Республики Башкортостан Рустам Муратов подписал документ по которому проект строительства логистического комплекса «Фармленд — Терминал 1» на территории Орджоникидзевского района вошел в Перечень приоритетных.
Агентство по инвестициям и развитию (KADI) в скором времени реализует уникальный в своем роде проект по выпуску лекарственных средств. Об этом сообщает финансовое издание Экономист со ссылкой на пресс-службу KADI.
Евразийская экономическая комиссия утвердила требования по исследованиям стабильности лекарственных растительных средств.
Совет Евразийской экономической комиссии согласовал пакет изменений в ранее принятые решения о введении маркировки товаров средствами идентификации.
Открыта онлайн-регистрация посетителей на международную специализированную выставку упаковочных технологий и оборудования upakovka 2022!
Евразийский межправительственный совет утвердил план мероприятий по повышению уровня обеспеченности государств — членов Евразийского экономического союза стратегически важными лекарственными препаратами и фармацевтическими субстанциями для медицинского применения.
Приглашаем посетить 29-ую международную специализированную выставку переработки и упаковки UPAKOVKA 2022, которая пройдёт с 25 по 28 января 2022 года на площадке ЦВК «Экспоцентр» в павильоне «Форум».
Министерство здравоохранения совместно с Министерством индустрии и инфраструктурного развития Республики Казахстан разработали Алгоритм реализации пилотного проекта оказания государственной услуги «Выдача сертификатов на соответствие надлежащих фармацевтических практик».
Три новых фармацевтических предприятия начнут работу в лабораторно-промышленных корпусах столичной особой экономической зоны (ОЭЗ) «Технополис Москва», сообщает пресс-служба столичного департамента инвестиционной и промышленной политики (ДИПП).
Административный центр острова Хайнань город Хайкоу объявил о запуске в эксплуатацию индустриальной площадки по обслуживанию современного фармацевтического оборудования.
Объем производства лекарств в России по итогам 1-3 кварталов 2021 года достиг 432,7 миллиарда рублей, что на 20% больше прошлогодних показателей.
Первый Международный форум «Global Pharm» по вопросам развития фармацевтической индустрии прошел в Казахстане, сообщает Официальный информационный ресурс Премьер-Министра Республики Казахстан